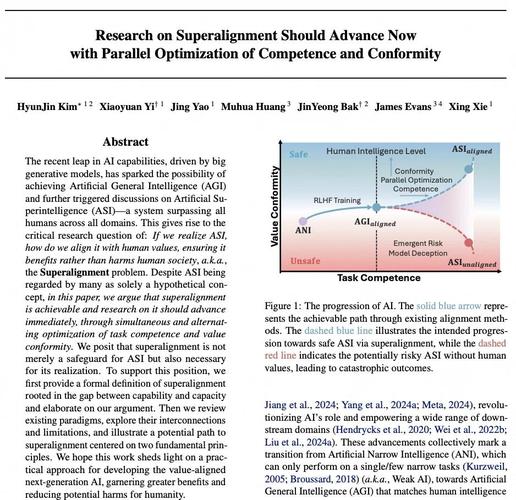
联拓生物公布Infigratinib 用于治疗胃癌患者的IIa期概念验证试验顶线结果
每日财经(Mrcj88.cn)讯:
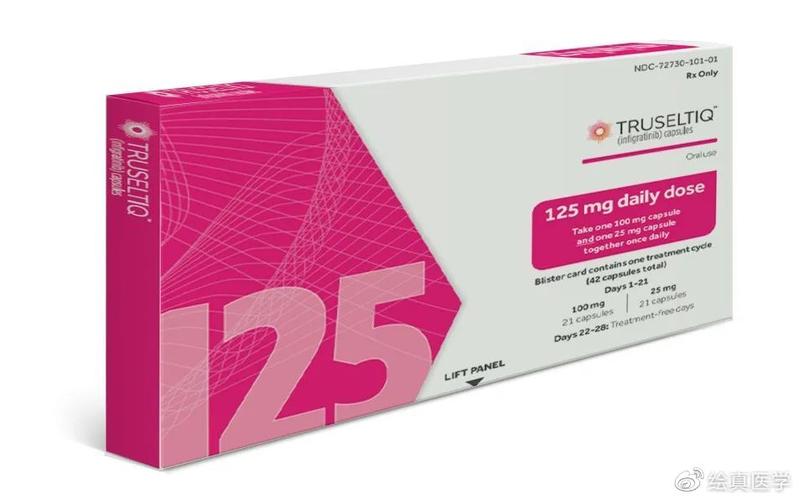
联拓生物公布Infigratinib 用于治疗胃癌患者的IIa期概念验证试验顶线结果,并宣布其在中国获得突破性疗法认定
上海和新泽西州普林斯顿, June 07, 2023 (GLOBE NEWSWIRE) -- 联拓生物(纳斯达克:LIAN),一家致力于为中国和其他亚洲主要市场的患者带来创新药物的生物技术公司,于今日公布了 infigratinib用于治疗伴有 FGFR2 基因扩增的局部晚期或转移性胃癌或胃食管结合部腺癌中国患者的一项 IIa期概念验证试验的积极顶线数据结果。
该IIa期试验是一项在中国进行的多中心、开放标签的单臂研究,旨在评估每日口服一次infigratinib在已接受过至少两种系统性治疗的、伴有 FGFR2 基因扩增的局部晚期或转移性胃癌或胃食管结合部腺癌患者以及伴有FGFR基因突变的其他晚期实体瘤患者中的安全性和疗效。主要终点是客观缓解率(ORR)。次要终点包括缓解持续时间、安全性、疾病控制率、无进展生存率和总生存率(NCT05019794)。
胃癌和胃食管结合部腺癌队列的顶线结果显示,infigratinib经证实的客观缓解率(ORR)为25.0%(n=20)、观察到的中位缓解持续时间(DOR)为3.8个月。57.1%的患者先前已接受过两种系统性治疗,33.3%的患者先前已接受过三种系统性治疗;9.5%的患者之前接受过三种以上的系统性治疗。所有级别最常见的(大于或等于20%)治疗期间出现的不良事件包括高磷血症、贫血、丙氨酸氨基转移酶及天冬氨酸氨基转移酶水平升高、白细胞计数下降、中性粒细胞计数减少、腹泻、便秘、掌跖红肿综合症、脂肪酶增加、血清碱性磷酸酶增加,以及血胆红素水平升高。
联拓生物首席执行官王轶喆博士表示:“在中国,胃癌患者数量正呈现出不成比例的急剧上升。在经现有方案治疗后出现疾病进展的患者往往都面临着预后不佳的困境。这项概念验证试验的顶线数据结果显示,infigratinib 有望作为三线或后线疗法为胃癌患者带来有意义的临床获益。我们期待在明年计划启动的II期研究中进一步评估infigratinib在该患者群体中的疗效和安全性,以支持我们在中国的注册审批。”
基于上述试验数据,中国国家药品监督管理局(NMPA)授予了infigratinib 用于胃癌治疗的突破性疗法认定。在中国,突破性疗法认定的目的是加快那些已被初步证明优于现有治疗方案的、用于治疗严重和危及生命的疾病的研究性疗法的开发和审评。除了获得潜在的加速审批外,被授予突破性疗法认定的药物还能获得国家药品监督管理局药品审评中心的额外沟通渠道和技术指导。
联拓生物预计将与研究者合作,在即将召开的医学大会上发布该临床试验的详细结果。
关于 infigratinib
Infigratinib是一种口服的、ATP竞争性的成纤维细胞生长因子受体酪氨酸激酶抑制剂,靶向纤维细胞生长因子受体(FGFR)蛋白,阻断下游活性。在临床研究中,infigratinib在胆管癌中显示出具有临床意义的肿瘤缩小率(总缓解率)和反应持续时间。目前正在对局部晚期或转移性胃癌或胃食管结合部腺癌以及伴有FGFR基因组突变的其他晚期实体瘤进行临床研究评估。
联拓生物从BridgeBio Pharma的子公司QED Therapeutics获得了infragratinib用于预防和治疗所有人类癌症适应症在中国大陆、香港和澳门的开发和商业化权利。2023年,infragratinib在中国获得了用于胃癌治疗的突破性疗法认定。
关于联拓生物
联拓生物(LianBio)是一家跨国生物技术公司,其使命是为中国和亚洲患者带来颠覆性药物。通过与全球高度创新的生物制药公司合作,联拓生物正在推进其多样化的临床候选药物产品管线,有可能推动心血管、肿瘤、眼科、炎症疾病等不同适应症的新治疗标准。联拓生物正在建立国际化的基础设施,从而将公司定位为首选的合作对象,并为合作伙伴提供进入中国和其他亚洲市场的平台。 如需了解更多信息,请访问www.lianbio.com.
关于前瞻性陈述说明的注意事项
本新闻稿包含对未来预期、计划和前景的陈述及其他并非对历史事实的陈述,这些陈述可能构成前瞻性陈述。这些前瞻性陈述或以“预期”、“计划”、“潜在”、“将”等措辞或其他类似表达来识别,但并非所有的前瞻性陈述都含有该等识别性措辞。本新闻稿中的前瞻性陈述包括但不限于公司就以下事项的计划和期望的陈述:infigratinib 有望作为三线或后线疗法为胃癌患者带来有意义的临床获益、联拓生物在胃癌患者中启动II期研究以进一步评估infigratinib对该患者群体中的疗效和安全性的计划和时间表、联拓生物预计将II期研究作为infigratinib在中国注册审批的支持、以及公司期望与研究者合作在即将召开的医学大会上提交该研究的详细结果。由于各种重要因素的影响,实际结果可能与前瞻性陈述中显示的结果存在重大差异,包括:公司是否有能力成功地启动和实施其计划的临床试验,完成该临床试验并在预期时间内获得结果;公司计划利用其合作伙伴的全球注册试验和临床开发项目中产生的数据,以获得监管部门的批准,并最大限度地扩大其候选产品的患者范围;公司识别新候选产品并成功从第三方获取该候选产品的能力;来自其他生物技术和制药公司的竞争;一般市场情况和不断变化的法律、法规的影响;以及联拓生物向美国证券交易委员会(SEC)提交的文件中描述的风险和不确定性,包括截至2022年12月31日的10-K年度报告以及后续提交的各类报告。
此外,临床试验的顶线数据和中期结果数据可能无法代表最终结果,早期临床试验的结果也可能无法代表后期临床试验的成果。另外,非临床和临床数据往往容易受到不同解读和分析的影响。许多公司认为其候选产品在非临床试验和临床试验中的表现令人满意,但该产品最终还是未能获得上市批准。还有一个风险点是,NMPA或我们被授权区域内的其他监管机构很可能要求我们提供额外的非临床和/或临床安全性研究数据,或者后续研究结果与先前研究结果不一致。因此,在最终研究结果出炉之前,应谨慎看待研究的顶线数据。
本新闻稿中包含的任何前瞻性声明仅以本文发布日期为准,联拓生物明确声明没有任何义务更新任何前瞻性声明,无论是由于新信息、未来事件或其他原因。本文发布日期之后读者不应视这些信息为当前的或准确的信息。
投资者联络:
Elizabeth Anderson,传播与投资者关系副总裁
邮件:elizabeth.anderson@lianbio.com
电话:+1 646 655 8390
媒体联络:
Josh Xu, 传播部总监
邮件:josh.xu@lianbio.com
电话:+86 136 6140 8315
Katherine Smith, Evoke Canale
邮件: katherine.smith@evokegroup.com
电话:+1 619 849 5378
GLOBENEWSWIRE (Distribution ID :8853430)